Researchers find method to regrow cartilage in the joints
In laboratory studies, Stanford School of Medicine researchers have found a way to regenerate the cartilage that eases movement between bones.
في دراساتهم المختبرية، وجد باحثو كلية الطب بجامعة ستانفورد طريقة لتجديد الغضروف مما يسهل الحركة بين العظام.
اكتشف باحثون في كلية الطب بجامعة ستانفورد طريقة لتجديد وسادة الغضروف الموجودة في المفاصل في الفئران والأنسجة البشرية. إن فقدان طبقة الأنسجة الزلقة والممتصة للصدمات، والتي تسمى الغضروف المفصلي، مسؤول عن العديد من حالات آلام المفاصل والتهاب المفاصل، التي تصيب أكثر من 55 مليون أمريكي، اذ يعاني ما يقرب من 1 من كل 4 أمريكيين بالغين من التهاب المفاصل، ويعاني أكثر من ذلك بكثير من آلام المفاصل والالتهابات بشكل عام.
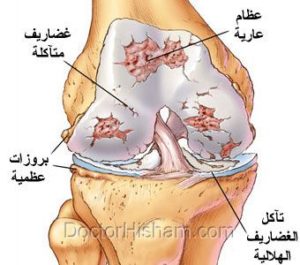
وقد اكتشف باحثو جامعة ستانفورد كيفية إعادة نمو الغضروف المفصلي عن طريق إحداث إصابة طفيفة في أنسجة المفصل أولا، ثم استخدام الإشارات الكيميائية لتوجيه نمو الخلايا الجذعية الهيكلية أثناء شفاء الإصابات. ونُشرت نتائج هذا العمل في 17 أغسطس في مجلة نايتشر ساينس Nature Medicine.
وقال الأستاذ المساعد في الجراحة الحاصل على درجة الدكتوراه، تشارلز كي اف تشان: “الغضروف ليس له أي قدرة على التجدد عمليًا في مرحلة البلوغ ، ولذلك بمجرد إصابته أو اختفائه، يكون ما يمكننا فعله للمرضى محدودًا للغاية؛ وإنه لمن دواعي سرورنا أن نجد طريقة لمساعدة الجسم على إعادة نمو هذا النسيج المهم”.

ويعتمد العمل هنا على أبحاث سابقة في جامعة ستانفورد أسفرت عن عزل الخلية الجذعية الهيكلية، وهي خلية ذاتية التجديد مسؤولة أيضًا عن إنتاج العظام، والغضاريف، ونوع خاص من الخلايا التي تساعد خلايا الدم على التطور في نخاع العظام. وتم اجراء البحث الجديد- مثل الاكتشافات السابقة للخلايا الجذعية الهيكلية للفئران والبشر- في الغالب في مختبرات تشان وأستاذ الجراحة مايكل لونجاكر.

والغضروف المفصلي هو نسيج معقد ومتخصص يوفر وسادة نطاطة وملساء بين العظام في المفاصل، وعندما يتضرر هذا الغضروف بسبب الصدمة أو المرض أو يخف ببساطة مع تقدم العمر، يمكن أن تحتك العظام ببعضها مباشرة، مسببًا الألم والالتهاب، الذي قد يؤدي في النهاية إلى التهاب المفاصل.
ويمكن معالجة الغضروف التالف من خلال تقنية تسمى الشرخ الدقيق، حيث يتم حفر ثقوب صغيرة في سطح المفصل؛ ويحث هذا الشرخ الدقيق الجسم على خلق أنسجة جديدة في المفصل، ولكن هذه الأنسجة الجديدة ليست مثل الغضروف. وقال تشان: ” ينتج عن الشرخ الدقيق ما يسمى بالغضروف الليفي، والذي يشبه النسيج الندبي أكثر من الغضروف الطبيعي؛ إنه يغطي العظام وهو أفضل من لا شيء، لكنه لا يتمتع بارتداد ومرونة الغضروف الطبيعي، ويميل إلى التدهور بسرعة نسبيًا”.
وقد نشأت أحدث الأبحاث، جزئيًا، من خلال عمل الجراح ماثيو مورفي ، الباحث الزائر في جامعة ستانفورد (وهو الآن في جامعة مانشستر). وقال الدكتور مورفي: “لم أشعر أبدًا أن أي شخص يفهم حقًا كيف تعمل الكسور الدقيقة حقًا، وأدركت أن الطريقة الوحيدة لفهم العملية هي النظر إلى ما تفعله الخلايا الجذعية بعد الكسر الدقيق”. [ مورفي هو المؤلف الرئيسي للورقة العلمية بمشاركة رئيسية من تشان ولونجاكر: https://www.nature.com/articles/s41591-020-1013-2].
وقال تشان: “لفترة طويلة، افترض الناس أن غضروف البالغين لم يتجدد بعد الإصابة، لأن الأنسجة لا تحتوي على العديد من الخلايا الجذعية الهيكلية التي يمكن تنشيطها؛ ومن خلال العمل في نموذج فأر، وثق الفريق أن الكسر الدقيق قد نشط الخلايا الجذعية الهيكلية. ومع ذلك، فقد قامت بتجديد الغضروف الليفي في المفصل، عندما تُركت هذه الخلايا الجذعية الهيكلية النشطة لأجهزتها الخاصة”.
ولكن ماذا لو تم توجيه عملية الشفاء بعد الشرخ الدقيق نحو تطوير الغضروف بعيدًا عن الغضروف الليفي؟ عرف الباحثون أنه مع نمو العظام، يجب أن تمر الخلايا أولاً بمرحلة الغضروف قبل أن تتحول إلى عظم. وكانت لديهم فكرة أنهم قد يشجعون الخلايا الجذعية الهيكلية في المفصل على بدء الطريق نحو أن تصبح عظامًا، لكنهم يوقفون العملية في مرحلة الغضروف.
واستخدم الباحثون جزيئًا قويًا يدعى بروتين تخلق العظام 2 (BMP2) لبدء تكوين العظام بعد الشرخ الدقيق، ولكنهم بعد ذلك أوقفوا العملية في منتصف الطريق بجزيء منع جزيء اشارة آخر مهم في تكوين العظام، يسمى عامل نمو بطانة الأوعية الدموية (VEGF).
وقال تشان: “ما انتهى بنا الأمر هو الغضروف الذي يتكون من نفس نوع الخلايا مثل الغضروف الطبيعي بخصائص ميكانيكية مماثلة، على عكس الغضروف الليفي الذي نحصل عليه عادة، كما أنه أعاد الحركة للفئران المصابة بالفصال العظمي وقلل من آلامها بشكل ملحوظ”.
وكدليل على أن هذا قد ينجح أيضًا في البشر، نقل الباحثون الأنسجة البشرية إلى الفئران التي تم تربيتها حتى لا ترفض الأنسجة، وتمكنوا من إظهار أن الخلايا الجذعية الهيكلية البشرية يمكن توجيهها نحو نمو العظام ولكن تتوقف عند مرحلة الغضروف.
وكانت المرحلة التالية من البحث إجراء تجارب مماثلة على الحيوانات الأكبر حجمًا قبل بدء التجارب السريرية البشرية. ويشير مورفي إلى أنه نظرًا لصعوبة العمل مع مفاصل الفئران الصغيرة جدًا، فقد يكون هناك بعض التحسينات على النظام التي يمكنهم إجراؤها أثناء انتقالهم إلى مفاصل أكبر نسبيًا.
وقد تجرى التجارب السريرية الأولى على البشر للأشخاص المصابين بالتهاب المفاصل في أصابع اليدين والقدمين. ويقول مورفي: “قد نبدأ بمفاصل صغيرة، وإذا نجح ذلك، فسننتقل إلى مفاصل أكبر مثل الركبتين، وفي الوقت الحالي، تعتبر إزالة العظام الموجودة في قاعدة الإبهام من أكثر العمليات الجراحية شيوعًا لالتهاب المفاصل في الأصابع، وفي مثل هذه الحالات، قد نحاول ذلك لإنقاذ المفصل، وإذا لم ينجح ذلك، فإننا نخرج العظم على أي حال. وهناك إمكانية كبيرة للتحسين، والجانب السلبي هو أننا سنعود إلى ما كنا عليه من قبل”.
ويشير لونجاكر إلى أن إحدى ميزات اكتشافهم هي أن المكونات الرئيسية للعلاج المحتمل تمت الموافقة عليها على أنها آمنة وفعالة من قبل إدارة الغذاء والدواء. وقال: “لقد تم بالفعل الموافقة على استخدام بروتين تخلق العظام 2 لمساعدة التئام العظام، وتستخدم مثبطات عامل نمو بطانة الأوعية الدموية (VEGF) بالفعل كما العلاجات المضادة للسرطان؛ وهذا من شأنه أن يساعد في تسريع الموافقة على أي علاج نطوره”.
وقد أحدثت جراحة استبدال المفصل ثورة في طريقة علاج الأطباء لالتهاب المفاصل وهي شائعة جدًا: بحلول سن الثمانين، سيتم استبدال مفصل الورك لواحد من كل 10 أشخاص واستبدال ركبة شخص واحد من كل 20 شخصًا. لكن مثل هذا الاستبدال هو إجراء جائر للغاية وله عمر محدود، ويتم إجراؤه فقط بعد إصابات التهاب المفاصل ومعاناة المرضى من قسوة الألم الدائم. ويقول الباحثون إن بإمكانهم تصور وقت يكون فيه الناس قادرين على تجنب الإصابة بالتهاب المفاصل في المقام الأول عن طريق تجديد غضروفهم في مفاصلهم قبل أن يتدهور بشدة.
وقال الدكتور لونجاكر: “تتمثل إحدى الأفكار في اتباع نموذج لوب جيفي (Jiffy Lube) لتجديد الغضروف، فأنت لا تنتظر حتى يتراكم الضرر، بل تنطلق بشكل دوري وتستفيد من هذه التقنية لتعزيز الغضروف المفصلي قبل أن تواجه مشكلة”.
*تمت الترجمة بتصرف
المصدر:
http://med.stanford.edu/news/all-news/2020/08/Researchers-find-method-to-regrow-cartilage-in-the-joints.html
الهوامش:
1 قاد هذا البحث العلمي البروفيسور مايكل لونجاكر وهو أستاذ في كلية الطب بجامعة ستانفورد والمدير المشارك لمعهد بيولوجيا الخلايا الجذعية والطب التجديدي، والأستاذ المساعد تشارلز كي اف تشان عضو في معهد بيولوجيا الخلايا الجذعية والطب التجديدي وعلم المناعة في جامعة ستانفورد، وشارك في البحث كل من الأساتذة والباحثين في جامعة ستانفورد: إيرفينغ وايزمان، أستاذ علم الأنسجة، وأستاذ في التحقيقات السريرية في أبحاث السرطان؛ ستيوارت ب. غودمان، أستاذ الجراحة؛ فان يانغ، أستاذ مساعد في جراحة العظام؛ شين مينغ تونغ، استاذ جراحة العظام؛ ديريك وان، أستاذ الجراحة؛ زينمنغ تونغ، أستاذ جراحة العظام؛ ثوماس البروسي، زميل أبحاث ما بعد الدكتوراه؛ ليمنغ زهاو، عالم زائر ما بعد الدكتوراه؛ لورن كويبكي وهولي ستينيجر، متخصصان في علوم الحياة؛ غونساغار غولاتي، طالب دكتوره؛ مالاتشيا هوفر، طالب الدراسات العليا؛ اوين ماريشيك، طالب سابق؛ يوتينغ وانغ، طالب طب سابق؛ الدكتور مارسين ووكيويشز، مدير مختبر المسح الضوئي والفحص المجهري.
2 تم دعم البحث من قبل: المعاهد الوطنية للصحة؛ معهد كاليفورنيا للطب التجديدي؛ مؤسسة أوك؛ صندوق بيتش جونسون؛ صندوق أبحاث غون / اوليفير؛ مؤسسة ستاينهارت / ريد؛ مؤسسة سيبل؛ معهد هوارد هيوز الطبي؛ مؤسسة الأبحاث الألمانية؛ الوقف الوطني لمؤسسة أبحاث الخدمة العامة ؛ المركز الوطني لمصادر البحث؛ مؤسسة أبحاث سرطان البروستاتا؛ الاتحاد الأمريكي لأبحاث الشيخوخة؛ مؤسسة أبحاث التهاب المفاصل الوطنية.
 علوم القطيف مقالات علمية في شتى المجالات العلمية
علوم القطيف مقالات علمية في شتى المجالات العلمية
