وردني قبل فترة سؤال عن فاعلية ثمرة كمثرى البلسم أو البطيخ المر اسمها العلمي (Momordica Charantia) او الاسم الدارج لها (bitter melon) وتأثيرها الإيجابي في خفض سكر الدم وفائدتها المحتملة في التحكم في مرض السكري النوع الثاني.
بعد بحث في الانترنت، وجدت بعض المعلومات التي تشير الى وجود آثار إيجابية لهذه الثمرة في تخفيض سكر الدم، ووجود بعض الدراسات الصغيرة الواعدة والتي تجعل منها علاجاً محتملاً للسكري.
[من وحي هذه الحادثة أحببت كتابة مقال، يتناول إمكانية تطوير أدوية علاجية من الأعشاب والنباتات الطبية بطرق حديثة، وما هي العقبات والتحديات التي تحول دون ذلك]

في البداية، أود سرد بعض المقدمات التوضيحية حول الدراسات الدوائية المطلوبة على أي دواء محتمل (في مثالنا النباتات الطبية) حتى يعتمد كدواء، من بداية اكتشاف الخصائص العلاجية المحتملة له، الى مرحلة وصوله للمريض، حتى تتضح الصورة:
1/ يوجد في الطبيعة الكثير من النباتات ذات الخصائص الطبية المعروفة من أعشاب وفواكه وخضروات، يعرف العلماء أن لها تأثير إيجابي معين (في مثالنا التحكم بسكر الدم) ، وهذا معروف إما من خلال الخبرات المتوارثة من القدماء، أو من بعض الدراسات الدوائية الحيوية الصغيرة الحديثة على الخلايا والحيوانات وعدد قليل من البشر، وهذه المعلومات المتعلقة بالنباتات الطبية، قد تجعلها أدوية محتملة للتحكم في مرض السكري.
لكن هذه المعلومات والدراسات ليست كافية لاعتبارها أدوية صالحة للاستخدام البشري المنتظم ووضعها ضمن التوصيات الإرشادية المعتمدة رسمياً، إذ لابد لها أن تجتاز رحلة طويلة وشاقة ومكلفة، من الدراسات العلمية بقسميها ما قبل السريري والسريري، وبعد أن تكملها بنجاح يمكن للجهات الطبية المختصة اعتمادها للاستخدام العلاجي ووضع توصيات إرشادية تنظم استخدامها.
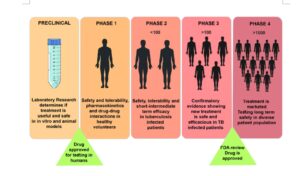
2/ تبدأ التجارب الدوائية الأولى، ( وهي المرحلة ما قبل السريرية) في تحديد المادة التي لها خصائص دوائية للتأثير العلاجي المطلوب. بعد ذلك يجري تحديد الجزء من النبات المحتوي لهذه المواد، سواء كان في الورقة أو الجذور أو الجذع أو القشرة أو البذور، بعد ذلك يجري العمل على معرفة طريقة استخلاص المادة الفعالة المطلوبة، وتحديد الصيغة الصيدلانية النهائية التي سيستعملها المريض، سواء كانت كبسولات أو شراب أو بودرة.
حيث لا يمكن صيدلانياً اعتماد الثمرة او العشبة الخام لعدة أسباب، منها صعوبة التعامل مع النبتة بشكلها الخام الكامل، لسرعة تلفها وزوال المادة الفعالة منها، نتيجة الرطوبة أو الحرارة أو أن المادة الفعالة في النبات الخام تركيزها قليل وقد يحتاج المريض تناول كميات كبيرة وهذا غير عملي، فضلاً على أنه قد يسبب ذلك تسمماً، أو أن المادة الفعالة لا يمكن الاستفادة منها بالشكل الأمثل إلا بعد بعض المعالجات البسيطة من غلي واستخلاص أو تجفيف وطحن وغيرها، ومن الأسباب المهمة كذلك، هو احتواء النبات غالباً على عدة مركبات فعالة حيوياً قد تعطي آثار متنافرة، وهذا قد يسبب فشل العلاج.
اذا اجتازت النبتة هذه المرحلة الأولية تجري عليها التجارب على الحيوانات. في هذه المرحلة الأولية، تجري التجارب لمعرفة التأثيرات العلاجية والآثار السمية والجرعة العلاجية والسامة والأعراض الجانبية على الحيوان.
3/ بعدها تأتي مرحلة التجارب على البشر. تُعرف هذه المرحلة باسم المرحلة 0 . وهي دراسات الجرعات الدقيقة البشرية. تشمل السمات المميزة لتجارب المرحلة 0 إعطاء جرعات علاجية فرعية واحدة من عقار الدراسة لعدد صغير من الأشخاص (10 إلى 15) لجمع البيانات الأولية عن الحرائك الدوائية للعامل، أي ما يفعله الجسم بالأدوية.
لا تعطي دراسة المرحلة 0 أي بيانات عن السلامة أو الفعالية، فهي بحكم التعريف جرعة منخفضة جدًا بحيث لا تسبب أي تأثير علاجي. تجري شركات تطوير الأدوية دراسات المرحلة 0 لتصنيف الأدوية المرشحة، من أجل تحديد أيها يحتوي على أفضل مؤشرات الحركية الدوائية في البشر للمضي قدمًا في مزيد من التطوير.
4/ بعد اجتياز العشب او غيره هذه المرحلة، واعتباره دواء محتمل للسكري في حالتنا ، تجري عليه تجارب اكلينيكية على عدد صغير من البشر 20-100 متطوع، تسمى دراسات أولية على الإنسان (first-in-human studies) لمعرفة خواصه الدوائية والعلاجية، ولتحديد الجرعة العلاجية والسامة والأعراض الجانبية، والسبب في ذلك اختلاف الاستقلاب والتمثيل الحيوي بين البشر والحيوانات، فقد يكون الدواء آمناً في الحيوانات، لكنه قد يكون ساماً على البشر بالجرعة العلاجية، وهذا يستبعده من كونه علاجاً، او انه يسبب أعراضاً جانبية خطيرة على أعضاء حيوية مثل القلب والكبد والكلى وغيرها، أو أن الجرعة العلاجية عالية جداً، وهذا قد يسبب الإسهال او القيء والغثيان أو غيره من الأعراض التي تمنع من اعتماده دواء، رغم خصائصه العلاجية على الخلايا والحيوانات. فسلامة الدواء أكثر أهمية من فائدته العلاجية.
يمكن تقسيم تجارب المرحلة الأولى بشكل أكبر [الدراسات الأولية على الإنسان]:
1/ الجرعة التصاعدية الواحدة (المرحلة الأولى 1A)
في دراسات الجرعة التصاعدية الواحدة، تعطى مجموعات صغيرة من الأشخاص جرعة واحدة من الدواء أثناء ملاحظتهم واختبارهم لفترة من الوقت لتأكيد السلامة. عادة، يدخل عدد صغير من المشاركين -عادة ثلاثة- بالتتابع بجرعة معينة. إذا لم تظهر عليهم أي آثار جانبية ضارة، وكانت بيانات الحرائك الدوائية متوافقة تقريبًا مع القيم الآمنة المتوقعة، ترفع (تصعد) الجرعة، ثم يعطى مجموعة جديدة من الأشخاص جرعة أعلى. إذا لوحظت سمية غير مقبولة في أي من المشاركين الثلاثة، يعالج عدد إضافي من المشاركين -عادة ثلاثة- بنفس الجرعة. يستمر هذا حتى يتم الوصول إلى مستويات أمان الحرائك الدوائية المحسوبة مسبقًا، أو تبدأ الآثار الجانبية التي غير المقبولة في الظهور، عند هذه النقطة يقال أن الدواء قد وصل إلى الحد الأقصى للجرعة المسموح بها (MTD). إذا لوحظت سمية إضافية غير مقبولة، عندئذٍ ينهى تصعيد الجرعة ويعلن عن تلك الجرعة، أو ربما الجرعة السابقة لها، على أنها أقصى جرعة يمكن تحملها.
2/ الجرعات التصاعدية المتعددة (المرحلة Ib)
تبحث دراسات الجرعات التصاعدية المتعددة في الحرائك الدوائية والديناميكيات الدوائية للجرعات المتعددة من الدواء، مع النظر في السلامة والتحمل. في هذه الدراسات، تتلقى مجموعة من المرضى جرعات منخفضة متعددة من الدواء، بينما تجمع عينات (من الدم والسوائل الأخرى) في نقاط زمنية مختلفة وتحليلها للحصول على معلومات حول كيفية معالجة الدواء داخل الجسم. ترفع الجرعة بعد ذلك لمجموعات أخرى، حتى مستوى محدد مسبقاً.

3/ بعد اجتياز الدواء المحتمل للمرحلة السابقة يدخل في الدراسات الاكلينيكية المرحلة الثانية: مرحلة بها عدد اكبر من المرحلة الأولى حوالي 20- 300 متطوع لتحديد الجرعة العلاجية والسامة وبعض الحرائك الدوائية وغيرها.
4/ بعد اجتياز هذه المرحلة تأتي المرحلة الثالثة، هذه المرحلة يجري اختبار الدواء بطريقة عشوائية ومراقبة على مجموعة أكبر بكثير من المراحل السابقة، (ما بين 300 إلى 3000 شخص) وقد تجري هذه المرحلة في عدة مراكز مختلفة لأعطاء نتائج أفضل للمادة الدوائية.
5/ بعد اتمام المراحل السابقة، وعندما يحصل مطور الدواء على أدلة من التجارب غير السريرية والسريرية تشير على ان الدواء آمن وفعّال، يجوز للشركة تقديم طلب لتسويق الدواء.
يتضمن طلب تسجيل دواء جديد سرد التفاصيل الكاملة للدواء، وعليه إظهار ان الدواء آمن وفعال. يحتوي هذا الطلب على كل المعلومات عن الدواء، من بيانات التجارب غير السريرية إلى بيانات المرحلة الثالثة في التجارب السريرية، بالإضافة إلى العلامة التجارية المقترحة، والمعلومات المتعلقة بالمريض، وتعليمات الاستعمال.
عندما يصل طلب تسجيل الدواء إلى المؤسسة التنظيمية الوطنية، يقرر فريق المراجعة إذا كان الطلب مكتمل ويبدأ عملية تحديد ما إذا يمكنهم الموافقة على الدواء. بالإضافة إلى المراجعة، قد يذهب مفتشو المؤسسة إلى مواقع التجارب السريرية لإجراء عمليات تفتيش. يقوم رئيس فريق المراجعة بجمع كل المراجعات والمستندات الفردية في حزمة عمل بمثابة السجل لمراجعة المؤسسة. يقوم فريق المراجعة بإصدار توصية ويتخذ المسؤول الاعلى في المؤسسة القرار النهائي في اعتماد الدواء من الجهات المختصة، تأتي مرحلة ما بعد التسويق أو مرحلة التوعية أو الرقابة الدوائية، فقد يسحب الدواء بعد تسويقه ، في حالة تسجيل حالات خطيرة من الأعراض الجانبية أو الوفاة.
تنبغي الإشارة الى أن عملية تطوير دواء جديد تتطلب استثماراً كبيراً في الوقت والمال، حيث قد تستغرق ما بين 10 الى 15 عاماً وقد تصل تكلفتها إلى أكثر من ملياري دولار حسب مؤشرات عام 2021. ربما المبلغ والمدة في المستقبل، نتيجة تطور التقنيات الحيوية الحديثة ومساعدة الذكاء الصناعي.
بعد هذه المقدمة الطويلة والضرورية، والتي أردت من خلالها توضيح العملية المعقدة والمضنية لتطوير أي دواء من بداية اكتشافة الى لحظة وصوله رف الصيدلية واستعمال المريض، وهو ما يؤكد بجلاء تعقيد وصعوبة العملية بمراحلها العديدة، واحتياجها الى جهد وأموال طائلة، وهذا ما لا تطيقه إلا الشركات الكبرى، ومؤكد أن هذه الشركات لن تقدم على عملية تطوير لدواء محتمل إلا إذا تأكدت من وجود احتمالية كبيرة من تحقيقها ارباحاً ونتائج واعدة من تلك العملية، لذلك لابد من التأكيد على صعوبة وندرة تطوير أدوية علاجية من الأعشاب والنباتات لأسباب عملية واقتصادية وقانونية مثل:
1/ العامل الاقتصادي
الأعشاب الطبية من نتاج الطبيعة ومتوفرة للجميع وليست مصنّعة ، لذلك فهي تفتقر لبراءة الاختراع او ما يسمى (patent) بحيث تملك الشركة المطوٍّرة للدواء حقوق حصرية في الإنتاج لمدة معينة، يضمن لها تحقيق الأرباح وتغطية تكاليف عملية التطوير والأبحاث، فغياب مثل هذا النوع من الملكية يحرم الشركات من احتكار المنتج، ما يجعل الشركات غير راغبة في إجراء الدراسات الاكلينيكية على النباتات الطبية كونها مكلفة جداً، حيث يصل تكلفة الدراسات الاكلينيكية الموسعة لعشرات ملايين الدولارات، وهذا يجعل حتى المراكز البحثية الرسمية غير قادرة على القيام بهذه الدراسات المكلفة والمعقدة ولغياب التمويل والدعم الكافي لها.
2/ العامل المتعلق بالأعشاب الطبية
لأن الأعشاب الطبية والأغذية منتجات طبيعية ، فهي محكومة بعوامل الطبيعة المتفاوتة والمختلفة، فلا يوجد تقييس أو نظام معياري دولي دقيق يضبط الأعشاب الطبية خلاف الأدوية الكيميائية المضبوطة والمعايرة جيداً بدساتير ومقاييس متعارف عليها دولياً.
الأعشاب الطبية بطبيعتها تحوي مواد كيميائية متعددة قد تصل لمئات المركبات، قد يتضارب مفعولها ويتداخل فيما بينها، مما يصعّب تحديد المادة الفعالة للأثر المعين، وحتى في حالة فصل المادة الفعالة المطلوبة، قد يختلف تركيزها بين العشبة الواحدة، لاختلاف الفصائل او المنطقة الجغرافية أو وقت الحصاد أو طريقة استخلاص المادة الفعالة أو طرق التخزين وغيرها من العوامل المؤثرة في جودة وفعالية المادة الفعالة في العشبة.
3/ العامل المتعلق بتصميم الدراسات الاكلينيكية
يوجد عامل مهم قد يحول دون نجاح الدراسات الاكلينيكية في الأعشاب ، وهو الاعتقاد القائم وراء المعالجة بالأعشاب بين كثير من المستهلكين للمنتجات الشعبية حول العالم، حيث يّتبع المعالجون (منهج الجسد والعقل) باعتبارهما شيئًا واحداً ومترابطاً تماماً، وهذا يستلزم الايمان والاعتقاد بالمعالِج وما يقدمه من علاجات. وهذا ليس المشكلة في حد ذاته، ولكنه مخالف لجوهر الدراسات الاكلينيكية في عدم التحيز والعامل النفسي المؤثر على النتائج ، مما يعيق التوصل إلى أن المادة المحددة هي سبب التأثير الفلاني بمعزل عن العوامل المؤثرة الأخرى. إذ أن الدراسات الإكلينيكية قائمة على مبدأ علمي واضح، وهو عامل استبعاد التحيز أو المصادفة أو العامل النفسي، لذلك تتميز الدراسات الإكلينيكية العشوائية المعمّاة المضبوطة (RCT) بأنها أقوى أنواع الدراسات الاكلينيكية وأكثرها أثراً ومصداقية، كونها تتغلب على عوامل المصادفة والتحيز.

4/ العامل المتعلق بسوق الأعشاب الطبية
يعاني سوق الأعشاب الطبية حالةً من الفوضى وضعف التنظيم، فكل ما يحتاجه مسوّق الأعشاب هو تسجيل منتجه لدى الجهات المختصة دون أن يُطلب منه توفير بيانات السلامة والفاعلية التفصيلية، بل يُكتفى بالحد الأدنى منها مثل شروط التصنيع الجيد ، بينما الحال في الأدوية يتوجّب على المنتج للدواء توفير المعلومات بتفاصيلها التي ذكرناها سابقاً لدى التسجيل عند السلطات الصحية. فاذا كان الحال كذلك من السهولة والبساطة، فلماذا يتجشّم منتج الأعشاب عناء إجراء الدراسات الإكلينيكية الصعبة والمكلفة، وهو يستطيع تسويق منتجه كمكل غذائي بكل سهولة.
خلاصة القول، ممارسة العلاج بالأعشاب ممارسة قديمة وعريقة ويستعملها مليارات البشر حول العالم في الماضي والحاضر، ولكن لا يمكننا الإتكاء على ما وصلنا من معلومات وخبرات سابقة من الماضي واعتبار الأعشاب البديل الفعال والآمن للأدوية المصنعة ، بدون إجراء الدراسات الاكلينيكية المطلوبة والتي اتبعناها طريقة موثوقة في اعتماد الأدوية.
توجد بعض الجهود الجادة في دول مختلفة مثل الهند والبرازيل وغيرها، لاستكشاف الفائدة العلاجية في الأعشاب ، لكنها كما أسلفنا عملية مكلفة وبطيئة ومعقدة، فحتى ذلك الوقت لا ينبغي الانجرار وراء الدعاوى العلاجية غير المثبتة التي يطلقها مسوّقوا الأعشاب الطبية دون وجود دليل علمي كاف يدعمها.

 علوم القطيف مقالات علمية في شتى المجالات العلمية
علوم القطيف مقالات علمية في شتى المجالات العلمية
