Beating Parkinson’s: Intense Exercise Regimen Helps Slow Disease Progression
(UNIVERSITA CATTOLICA DEL SACRO CUOREبواسطة: الجامعة الكاثوليكية للقلب المقدس الايطالية – (ميلان))
ملخص المقالة:
وجد علماء أعصاب ايطاليون أن التمارين المكثفة يمكن أن تبطئ من تطور مرض باركنسون، كما قاموا أيضًا بوصف الآليات البيولوجية الكامنة وراء العملية التي من خلالها تؤدي التمارين في المراحل المبكرة من المرض إلى تأثيرات مفيدة على التحكم في الحركة والتي قد تستمر بمرور الوقت حتى بعد تعليق التدريب. وقد أشارت الأبحاث السابقة إلى أن النشاط البدني المكثف كان مرتبطًا بزيادة إنتاج عامل النمو الحيوي، وهو عامل التغذية العصبية المشتق من الدماغ. ويمكن أن تقود نتيجة ابحاث العلماء الايطاليين الحالية الى تطوير علاجات جديدة غير دوائية لاستخدامها جنبًا إلى جنب مع العلاجات الدوائية الحالية.
( المقالة )
يمكن أن يؤدي التمرين المكثف إلى إبطاء تطور مرض باركنسون من خلال تحسين مرونة الدماغ وبقاء الخلايا العصبية، وفقًا لدراسة بحثية من الجامعة الكاثوليكية (حرم روما الجامعي) ومؤسسة مستشفى اغيستينو غيميللي الجامعي العام (A. Gemelli IRCCS Polyclinic Foundation). وقد تقود النتائج الى تطوير علاجات غير دوائية للمرض.

نتائج جديدة في أبحاث باركنسون
وجد علماء الأعصاب في كلية الطب بالجامعة الكاثوليكية (حرم روما الجامعي) ومستشفى اغيستينو غيميللي الجامعي العام أن التمارين المكثفة يمكن أن تبطئ من تطور مرض باركنسون. وقد وصفوا أيضًا الآليات البيولوجية الكامنة وراء هذه العملية، مما يوفر طرقًا محتملة لنهج العلاج غير الدوائية الجديدة.
وقد نُشرت الدراسة البحثية، التي تحمل عنوان “التمرين المكثف يخفف من الأعراض الحركية والإدراكية في مرض باركنسون التجريبي من خلال استعادة اللدونة التشابكية المخطط لها” ، في 14 يوليو 2023 في مجلة “ساينس ادفانسز” (Science Advances). وقاد التحقيق الجامعة الكاثوليكية (حرم روما الجامعي)، ومستشفى اغيستينو غيميللي الجامعي العام، بالتعاون مع العديد من المعاهد البحثية بما في ذلك جامعة سان رافاييل عن بعد في روما، والمجلس الوطني للبحوث في ايطاليا[1] (National Research Council (CNR))، ومعهد تيليثون للوراثة والطب[2] (Telethon Institute of Genetics and Medicine (TIGEM))، وجامعة ميلانو، ومعهد سان رافاييل العلمي للبحوث والاستشفاء والرعاية الصحية[3] (IRCCS San Raffaele) في روما.
التمويل والآثار
تم تمويل هذا البحث من قبل معهد فريسكو باركنسون (في ايطاليا)، وكلية الطب بجامعة نيويورك، ومعهد مارلين وباولو فريسكو لاضطرابات باركنسون والحركة (في نيويورك)، ووزارة الصحة الايطالية ووزارة التربية والتعليم الايطالية (منحتان مختلفتان). وكشفت الدراسة عن آلية جديدة تشرح الآثار المفيدة للتمرين على لدونة الدماغ.
وقال البروفيسور باولو كالابريسي، الأستاذ الكامل لطب الأعصاب في الجامعة الكاثوليكية ومدير طب الأعصاب في مستشفى اغيستينو غيميللي الجامعي العام: “لقد اكتشفنا آلية لم تتم ملاحظتها أبدًا، والتي من خلالها تؤدي التمارين التي يتم إجراؤها في المراحل المبكرة من المرض إلى تأثيرات مفيدة على التحكم في الحركة والتي قد تستمر بمرور الوقت حتى بعد تعليق التدريب”. وأضاف أن هذه النتيجة يمكن أن تقود الى تطوير علاجات جديدة غير دوائية لاستخدامها جنبًا إلى جنب مع العلاجات الدوائية الحالية.
المعرفة السابقة والأدلة الجديدة
أشارت الأبحاث السابقة إلى أن النشاط البدني المكثف كان مرتبطًا بزيادة إنتاج عامل النمو الحيوي، وهو عامل التغذية العصبية المشتق من الدماغ. وقد نجح المؤلفون في تكرار هذه الظاهرة باستخدام بروتوكول تدريب على جهاز المشي لمدة أربعة أسابيع في نموذج حيواني لمرض باركنسون في مراحله المبكرة. ولأول مرة، أثبتوا كيف يساهم عامل التغذية العصبية هذا في الآثار المفيدة للنشاط البدني على الدماغ.
التحقيق في تأثير الحماية العصبية
بقيادة الدكتورة جيويا مارينو والدكتورة فيديريكا كامبانيللي، الباحثتان في كلية الطب بالجامعة الكاثوليكية في روما، تقدم الدراسة دعمًا تجريبيًا للتأثير الوقائي العصبي للتمرين. وقد استخدموا نهجًا متعدد التخصصات باستخدام تقنيات مختلفة لقياس التحسينات في بقاء الخلايا العصبية، ولدونة الدماغ، والتحكم الحركي، والإدراك البصري المكاني.
وكانت الملاحظة الرئيسية هي أن الدورات التدريبية اليومية على جهاز المشي قللت من انتشار مجاميع ألفا-سينوكلين[4] المرضية. وفي مرض باركنسون، تسبب هذه المجاميع خللًا تدريجيًا وتصاعديًا في الخلايا العصبية في مناطق معينة من الدماغ (المادة “نيغرا بارس كومباكتا”[5] و”سترياتوم”[6] – المكونة لما يسمى بمسار “نيغروسترياتال”[7]) الضروري للتحكم الحركي.
فهم الآلية البيولوجية
يرتبط التأثير الوقائي للنشاط البدني ببقاء الخلايا العصبية التي تطلق دوبامين الناقل العصبي. وهذا البقاء على قيد الحياة أمر حاسم لقدرة الخلايا العصبية “سترياتال” على التعبير عن شكل من أشكال اللدونة (Plasticity) المعتمدة على الدوبامين، والتي يضعفها المرض. ونتيجة لذلك، يتم الحفاظ على التحكم الحركي والتعلم البصري المكاني المعتمدين على نشاط “نيغروسترياتال” في الحيوانات التي تخضع لتدريب مكثف.
كشفت الدراسة أيضًا أن عامل التغذية العصبية المشتق من الدماغ، الذي ترتفع مستوياته مع التمرين، يتفاعل مع مستقبل إن-ميتيل-دي-اسبارتيت[8] (N-methyl-D-aspartate (NMDA)) للغلوتامات[9]. يمكّن هذا التفاعل الخلايا العصبية في المخطط من الاستجابة بفعالية للمنبهات ، مع تأثيرات تستمر إلى ما بعد فترة التمرين.
التطلع إلى المستقبل
قال البروفيسور باولو كالابريسي: “يشارك فريق البحث لدينا في تجربة إكلينيكية لاختبار ما إذا كانت التمارين المكثفة يمكن أن تحدد علامات جديدة لمراقبة تطور المرض الذي يتباطأ في مرضى المراحل المبكرة ومراقبة ملف تطور المرض. ونظرًا لأن مرض باركنسون يتميز بمكونات مهمة للالتهابات العصبية والمناعة العصبية، والتي تلعب دورًا رئيسيًا في المراحل المبكرة من المرض، فسوف يستمر البحث في التحقيق في مشاركة الخلايا الدبقية، وهي مجموعات عالية التخصص من الخلايا التي توفر الدعم المادي والكيميائي للخلايا العصبية وبيئتها. وسيتيح لنا ذلك تحديد الآليات الجزيئية والخلوية الكامنة وراء الآثار المفيدة المرصودة”.
*تمت الترجمة بتصرف
المرجع: “Intensive exercise ameliorates motor and cognitive symptoms in experimental Parkinson’s disease restoring striatal synaptic plasticity” by Gioia Marino, Federica Campanelli, Giuseppina Natale, Maria De Carluccio, Federica Servillo, Elena Ferrari, Fabrizio Gardoni, Maria Emiliana Caristo, Barbara Picconi, Antonella Cardinale, Vittorio Loffredo, Francesco Crupi, Elvira De Leonibus, Maria Teresa Viscomi, Veronica Ghiglieri and Paolo Calabresi, 14 July 2023, Science Advances. DOI: 10.1126/sciadv.adh1403
المصدر:
الهوامش:
[1] المجلس الوطني للبحوث في إيطاليا (CNR) هو أكبر مؤسسة بحثية عامة في إيطاليا وهو منظم في أقسام ومعاهد. [2] معهد تيليثون للوراثة والطب (TIGEM) هو معهد أبحاث متعدد التخصصات مكرس لدراسة الآليات الكامنة وراء الأمراض الوراثية النادرة وتطوير علاجات مبتكرة. [3] تم الاعتراف بمعهد سان رافاييل العلمي للبحوث والاستشفاء والرعاية الصحية (اختصار بالإيطالية IRCCS) في عام 2005 من قبل وزارة الصحة الإيطالية كمعهد أبحاث في مجال إعادة التأهيل الحركي والحسي في مجالات مختلفة من الطب: أمراض القلب، وأمراض الرئة، والأنف والأذن والحنجرة، وطب الأعصاب، وجراحة العظام، وإعاقات النمو. المعهد به 298 سريرا موزعة على المرضى الداخليين العاديين والمستشفيات النهارية. [4] يشارك تجمع ألفا سينوكلين (αS) في الأمراض التنكسية العصبية بما في ذلك مرض باركنسون، وضمور الجهاز المتعدد، والخرف مع أجسام ليوي (Lewy)، ولكن لا يوجد إجماع على الآليات التي تؤدي إلى التجميع، وفقدان الخلايا العصبية، والتنكس. تشكل مجاميع ألفا سينوكلين أوليغومرات سامة وخيوط أميلويد تسمى أجسام ليوي. إن وجود سلالة معينة من ألفا سينوكلين تسبب ضمورًا ضمور جهازيا متعددًا، وسلوك بذوري، وتضخيم سلالات ألفا سينوكلين معينة يهيمن على مفهوم البريون في التنكس العصبي. المصدر: https://www.nature.com/articles/s42003-019-0598-9ويشير مصطلح “البريون” إلى عوامل غير طبيعية وممرضة قابلة للانتقال وقادرة على إحداث طي غير طبيعي لبروتينات خلوية طبيعية معينة تسمى بروتينات البريون الموجودة بكثرة في الدماغ. المصدر: https://www.google.com/search؟q=prion+concept&source
[5] المادة “نيغرا” هي جزء من الدماغ يساعد في التحكم في الحركات. إنها جزء من العقد القاعدية، وهي مجموعة من الهياكل التي تشكل روابط ودوائر في جميع أنحاء الدماغ. هذه المادة مهمة بسبب دورها في الحركة وتأثيرها على كيمياء العقل. المصدر: https://my.clevelandclinic.org/health/body/23010-substantia-nigra-sn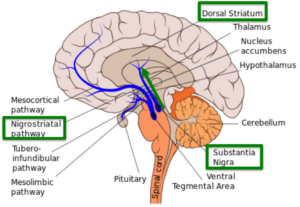

 علوم القطيف مقالات علمية في شتى المجالات العلمية
علوم القطيف مقالات علمية في شتى المجالات العلمية
