تستضيف أجسامنا تريليونات الكائنات الحية الدقيقة، التي يفوق عدد خلاياها خلايا الجسم نفسه. وتتكوَّن هذه من البكتيريا والفيروسات والفطريات واليوكاريوت الدقيقة، وتُعرف مجتمعةً باسم (microbiota) “الميكروبيوتا”، في حين يُستخدم المصطلح (microbiome) “ميكروبيوم” لوصف الكائنات الحية الدقيقة، بالإضافة إلى عناصر المضيف المستمدة من مكوّنات البيئة التي تعيش فيها هذه الكائنات الحية الدقيقة.
يقوم الميكروبيوم بعدة وظائف منها، هضم الطعام، وإنتاج بعض الفيتامينات، وتنظيم جهاز المناعة، وحماية بعض أنواعها الحميدة لنا من بعضها الآخر المسبب للأمراض. ولو أزلنا كل الميكروبات التي تسكن جسدنا فسنخسر قرابة كيلوغرامين من وزننا، لكنك أيضًا سنكون عرضةً للعديد من الأمراض والأزمات الصحية.
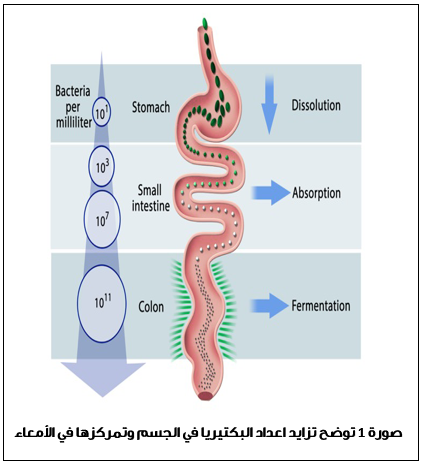
تظل الأجنّة معقَّمة طبيعياً حتى لحظة ولادتها من خلال قناة الولادة، حيث تتعرَّض للميكروبيوم المهبلي. هذا يمثل التأسيس المبكر لميكروبيومات هذه الأجنّة التي تستمر بالتطور خلال السنوات الأولى من الحياة متأثرة بالميكروبيوتا الموجودة في حليب الأم والكائنات الحية الدقيقة الموجودة في البيئة، كما تتأثر كذلك بالتعرُّض للمضادات الحيوية.
تداخل ميكروبيوم الأمعاء بوظائف الجهاز العصبي
على مدى العشرين عاماً الماضية، أثبتت الأدلة أن التغييرات في ميكروبيوتا الأمعاء، يمكن أن تغير بشكل كبير فسيولوجيا الدماغ وسلوكه.
لبكتيريا الأمعاء تأثيرات مباشرة وغير مباشرة على وظائف الدماغ، وفي النهاية على السلوك من خلال كثير من الآليات المعقدة؛ حيث تنتج الميكروبات، وتطلق نواتج الأيض والجزيئات الأخرى، التي تدخل الدورة الدموية وتؤثر على العمليات الجسدية القريبة والبعيدة. وبعض المواد الميكروبية، مثل مادة «التربتوفان» المؤثرة على النوم و «اللبتين» المنظم للشهية، هي مواد نشطة عصبياً بشكل مباشر. والمشتقات الحيوية الأخرى للأمعاء، مثل الأحماض الدهنية قصيرة التسلسل التي يتم إطلاقها من خلال هضم الكربوهيدرات التي يمكن للجراثيم (MACs) الوصول إليها.
البروبيوتيك وعلاقته بصحة الميكروبيوم
البروبيوتيك، هي مزيج من البكتيريا الحية التي تمنح فوائد صحية عند تناولها بكميات مناسبة.
تبلغ قيمة هذه الصناعة مليارات الدولارات، ومن المتوقع أن ترتفع. الغالبية العظمى من البروبيوتيك تندرج تحت فئة المكملات الغذائية ولا تخضع للتنظيم. ونتيجة لذلك، إن تكوين هذه العناصر المتوفرة تجارياً، وتأثيرها على ميكروبيوتا الأمعاء لم تُدرس بشكلٍ كافٍ حتى الآن.

البريبايوتيك هي نوع من الكربوهيدرات المتوفرة في أجزاء الطعام غير القابلة للهضم التي تتغذي عليها الأمعاء فقط، وهي تحفز نمو البكتيريا النافعة ونشاطها.
؛؛لا تحتوي البريبايوتيك على بكتيريا نافعة، لكنها تعد مصدر الوقود والغذاء بالنسبة لها؛؛
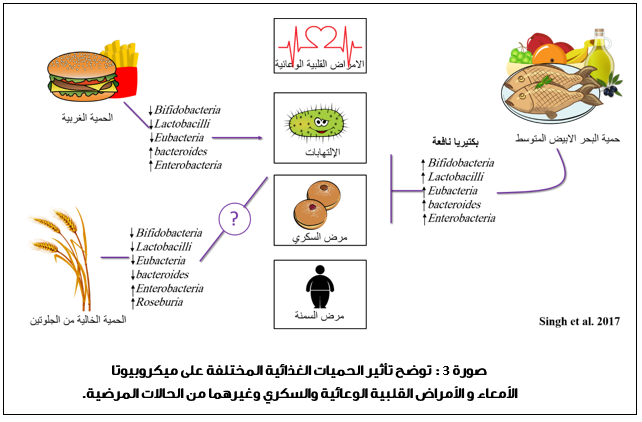
تمر ألياف البريبايوتيك عبر الأمعاء الدقيقة دون هضم، وعندما تصل إلى الأمعاء الغليظة تخضع لعملية التخمير التي توفر الغذاء للبكتيريا النافعة وتساعد في زيادة عددها في الجهاز الهضمي.
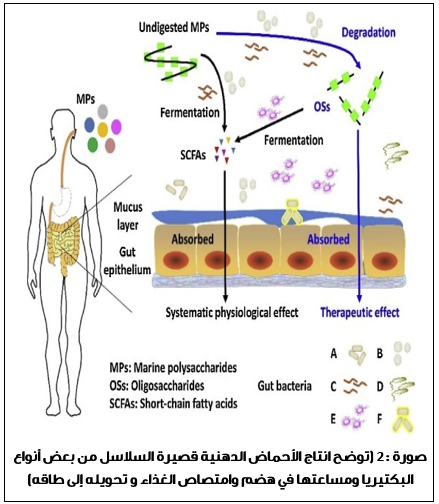
تأثير اختلاف النمط الغذائي على ميكروبيوم الأمعاء
أظهرت الدراسات في امريكا، التي أجريت على مدار العامين الماضيين، أن الهجرة إلى الولايات المتحدة مصحوبة دوماً بتغييرات هائلة في ميكروبيوم الأمعاء (gut microbiome)، ولا سيما التغييرات في تركيبته وبنيته، مع تأثيرات بعيدة المدى. وقد وثّق الباحثون فقدان التنوع البكتيري، ومحو سلالات كاملة من الجراثيم (ولا سيما التي تنتمي إلى فصيلة بريفوتيلا “Prevotella genus”)، وفقدان أدائه المهام، بما في ذلك القدرة على معالجة الكربوهيدرات والألياف بشكل كامل.
أشارت الدراسات التي أجريت على الحيوانات إلى أن تناول نسبة عالية من البروتين المشتق من الحيوانات، مقارنة بالكربوهيدرات، يمكن أن تغير الميكروبيوم في يوم واحد، ما يضع جرثومة بريفوتيلا على طريق الانقراض.
ويُعتقد أن التغييرات، ولا سيما فقدان التنوع البكتيري، هي المسؤولة عن معدلات السمنة المتزايدة التي لوحظت بشكل لافت للنظر في المهاجرين الأميركيين على مدى العقود الكثيرة الماضية، وهي الفترة التي تحوّل فيها النظام الغذائي الأميركي بشدة إلى الأطعمة المصنعة، واللحوم الحمراء عالية الدهون، بعيداً عن الأطعمة الغنية بالألياف المليئة بالكربوهيدرات المعقدة، والمعروفة أيضاً باسم الكربوهيدرات التي يمكن للجراثيم (MACs) الوصول إليها.
علم الأدوية الميكروبيومي “Pharmacomicrobiomics”، علم جديد وواعد
تسلك العقاقير التي نتناولها عن طريق الفم مسارًا يمر بالمعدة ومنها إلى الأمعاء، حيث تلتقي بمجتمع متنوع من الميكروبات المتوطنة فيها، بل قد تجد العقاقير التي تُعطى عبر مسالك أخرى (مثل الحقن) طريقَها إلى الأمعاء أيضًا، حيث تستقلب في الكبد ثم تفرز في العصارة الصفراوية إلى المرارة ومنها إلى الأمعاء الدقيقة.
؛؛قد يبدل تفاعل العقاقير مع الميكروبيوم من خصائصها، فيزيد أو يقلل من فاعليتها، ويحدد مدى سمِّيَّتها؛؛
ولأن لكل شخص تكوينًا فريًدا من الميكروبيوم؛ تُعد دراسة تفاعله مع العقاقير مبحثًا مهمًّا نحو تطوير خطط علاجية مصممة وفق طبيعة كل فرد، وهو اتجاه طبي حديث يُعرف بالطب الدقيق.
الميكروبيوم يفتح بُعداً جديداً للطب الدقيق
بنهاية التسعينيات كانت الشركات الدوائية تستعد لحقبة جديدة من الأبحاث الدوائية، كان من الثابت أن جيناتنا تؤدي دورًا في مدى فاعلية العقاقير، وكانت جهود مشروع الجينوم البشري الهادفة إلى قراءة كامل تتابُع المادة الوراثية للبشر قد قاربت على تحقيق مبتغاها.
عزَّز المشروع بعد انتهائه عام 2001 تقدُّم علم الأدوية الجينومي، وهو العلم الذي يدرس تأثير الفروق الجينية بين الأفراد على فاعلية العقاقير وسلامتها، وهو ما عُد حجرَ أساس للطب الدقيق.
وتتراوح معدلات الاستجابة بين الأفراد لبعض العقاقير الشائعة بين 50% و 75% وفق بعض التقديرات.
كان من الواضح بعد انتهاء مشروع الجينوم البشري أن المتغيرات في جيناتنا وحدها لا تستطيع تفسير اختلاف استجابة الأفراد للعقاقير؛ إذ يقبع الكم الأكبر من الجينات داخل الميكروبيوم”.
تقدر الدراسات أن عدد الجينات التي يحويها الميكروبيوم يزيد على عدد الجينات البشرية بأكثر من 100 ضِعف، وهناك عدد متزايد من الأدلة التي تبرهن تأثيرها على العقاقير.
دراسة مصرية رائدة في مجال علم الأدوية الميكروبيومي
جمع الفريق البحثي في مصر عينات براز من 16 متطوعًا من الأصحاء المصريين، إذ يحمل البراز ميكروبات الجهاز الهضمي، لم يكن لدى هؤلاء الأشخاص أمراض مزمنة أو معدية، وليس لديهم تاريخ سابق لأمراض الجهاز الهضمي، واشترط الفريق البحثي ألا يكون المتطوعون قد تناولوا أي مضاد حيوي لمدة 3 أشهر قبل وقت جمع العينة؛ حتى لا يؤثر على تكوين الميكروبيوم.
ركز الفريق في دراسته على عائلة من الإنزيمات الميكروبية تُعرف بـ”الآزوريدكتاز”. في الوقت ذاته، عزل الفريق المادة الوراثية الخاصة بالميكروبات من عينات البراز، ليُجري عليها اختبارًا وراثيًّا يمكن من خلاله تحديد الشعب الرئيسية للبكتيريا الموجودة في كل عينة.
إلا أن الباحث ينوه بأن النتائج أولية، إذ من الضروري زيادة عدد العينات، وجمعها من مناطق جغرافية مختلفة ومن أشخاص ذوي نمط غذائي متنوع؛ للتأكد مما أشارت إليه نتائج الدراسة.
علق أحد الخبراء على الدراسة: “في حين أن الدراسة أولية ووصفية في مبحثها، إلا أنها تأسيسية؛ إذ تطرح فرضيةً عن سبب اختلاف نشاط نوع من الإنزيمات المعدلة للعقاقير بين الأفراد، لتفتح الباب للمزيد من الدراسات الموجهة إلى تلك النقطة”.
ويضيف الباحث: “نحتاج إلى المزيد من الدراسات الكاشفة لتكوين الميكروبيوم عند المصريين حتى الوصول إلى مرحلة يمكن فيها ترجمة تلك المعرفة إلى تدخلات طبية؛ إذ يمثل ذلك بُعدًا حديثًا للطب الدقيق”.
ما طبيعة التدخلات العلاجية الممكنة؟
إذا توافرت معرفة كافية بتفاعلات الميكروبيوم مع العقاقير، فسيكون من الممكن فحص الميكروبيوم لكل مريض قبل تحديد الخيار العلاجي، وعلى أساسه يتم تحديد أي العقاقير سيكون أكثر فاعلية، وتركيز الجرعة المناسبة لكل فرد، وكذلك تجنُّب الخيارات العلاجية التي قد تتسبب في أعراض جانبية حادة لدى بعض المرضى.
على خلاف الجينات البشرية، فإن “الميكروبيوم ذاته قابل للتعديل”، باستخدام مضادات حيوية محددة أو تغيير النمط الغذائي أو ربما حث المريض على تناول مكملات تحوي ميكروبات نافعة (معززات حيوية probiotics) يمكن تغيير تكوين الميكروبيوم بهدف زيادة استجابة المريض للعلاج.
“من الممكن أيضًا استهداف إنزيمات خاصة بالميكروبيوم دون تغييره” وتبين دراسات أُجريت على الفئران أن تثبيط إنزيمات خاصة بأنواع من ميكروبات الأمعاء، مثلاً يمكنه تقليل الآثار الجانبية الحادة لعقار “إرينوتيكان”، الذي يُستخدم لعلاج سرطان القولون.
تكشف الدراسات الوراثية أن لكل إثنية (عرق أو أصل معين) بعض المتغيرات الجينية الفريدة التي قد ترتبط بأمراض محددة، أو بالاستجابة للعقاقير،
يختلف تكوين الميكروبيوم بين الإثنيات وسكان الدول المختلفة حول العالم، وهو ما قد يحد من فاعلية التدخلات الطبية المبنية على الميكروبيوم في الجماعات أو الإثنيات التي لم تُدرس بشكل كافي، وفق ما أوضحه باحثون في في دورية “Frontiers in Microbiology” عام 2017.
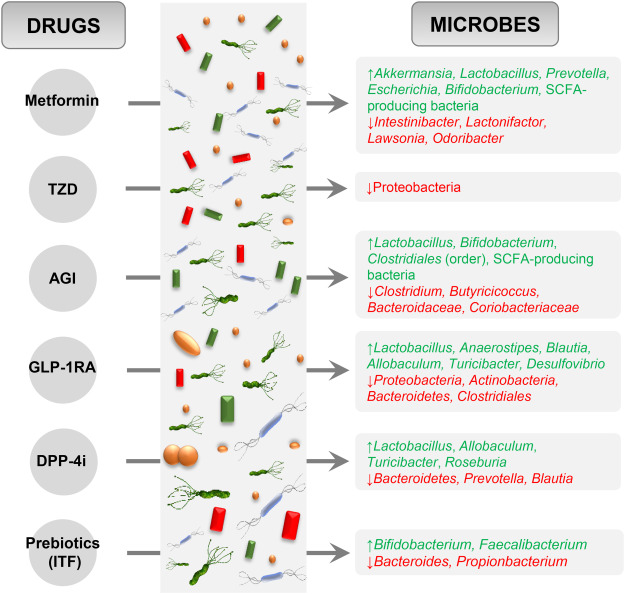
تأثير بعض الأدوية على بكتيريا القولون
في الختام، دراسات الميكروبيوم مجال بحثي واسع وواعد، وتجري عليه حالياً آلاف الدراسات سنوياً، ولذلك ينبغي الاهتمام الكبير بهذا المجال محلياً وإعطائه قدراً من الاهتمام، كونه سيشكل مدخلاً مهماً إلى مجالات عدة في التغذية والتشخيص والعلاج.
*غسان علي بوخمسين ، صيدلاني أول ، مستشفى جونز هوبكنز.
 علوم القطيف مقالات علمية في شتى المجالات العلمية
علوم القطيف مقالات علمية في شتى المجالات العلمية

مقال مفيد .. تشكر دكتور على هذه المعلومات .. اضيف ايضا تأثير البروبيوتك على متلازمة ارتشاح الأمعاء leaky gut syndrome عن طريق تحسين وجود الميكروبات النافعة في الجهاز الهضمي و بالتالي التقليل من الارتشاح .. و هذا يزيد من التحسن والتعافي من كثير من الامراض منها الحساسية المفرطة و التوحد و غيرها
شكراً لك د مصطفى على القراءة والتعليق، جواباً على سؤالك، يرى العديد من الخبراء أن نظرية الأمعاء المرتشحة أو المتسربة، نظرية غير ناهضة وليس لها أدلة تسندها ؛ لذلك لم أتعرض لها في المقال؛ كونها قضية خلافية ويتهمها البعض أنها من ابتكارات الطب البديل وليس لها أساس في الطب الذي نعرفه حسب قراءاتي.
بل حتى البروبيوتيك قيل عنها الكثير في فوائدها العلاجية المُدعاة، ولكن لم يثبت شيء منها، حسب الدراسات الإكلينيكية القليلة التي أجريت عليها، وهذا يطرح التساؤل عن الفرق بين البكتيريا النافعة في الغذاء والمكملات الغذائية، لذلك أشدد مرةً أخرى على ما ذكرته في نهاية المقال، بأننا بحاجة لمزيد من الدراسة والبحث للتعرف على هذا العالم الخفي والعجيب والذي له الأثر الكبير على صحتنا ومرضنا.
غسان بوخمسين / كاتب المقال