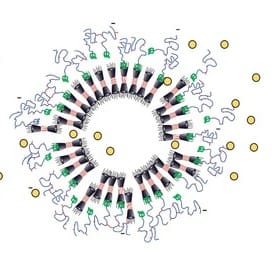
Newly developed, bioinspired cell delivery vehicles
[University of Münster – مقدمة: من جامعة مونستر (الألمانية)]
ملخص المقالة:
طور العلماء في جامعة مونستر (بألمانيا) نوعًا جديدًا من الحاويات النانوية التي تم إنشاؤها بالكامل من مكونات بيولوجية. وتعتمد على مركبات السكر التي يتم غلقها بقشرة من الهياكل البروتينية (البولي ببتيدات) التي يتم تفصيل سمكها بدقة. وتتحلل قشرة الحاوية داخل الخلية بفعل أنزيمات الخلية، ويتم نتيجة لذلك إفراغ المواد المنقولة بسرعة بمجرد وصولها إلى الخلية.
( المقالة )
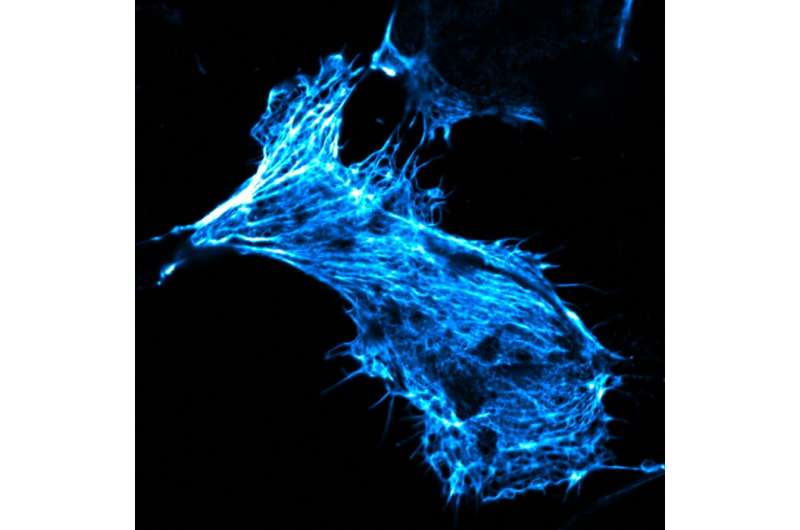
يمكن للحاويات النانوية نقل المواد الى داخل الخلايا حيث يمكن أن تصبح مؤثرة بعد ذلك. وهذه هي الطريقة المستخدمة في لقاحات الحمض الريبي المرسال (mRNA)، على سبيل المثال، المستخدمة حاليًا ضد كوفيد-19 وكذلك بعض أدوية السرطان. وفي البحث، يمكن أيضًا استخدام ناقلات مماثلة لإيصال المواد المصنفة إلى الخلايا لدراسة الوظائف الخلوية الأساسية. وللاستفادة من إمكاناتهم الكاملة، يُجري العلماء بحثًا مكثفًا حول كيفية تفاعل الحاويات النانوية مع البيئات البيولوجية وكيف يجب أن يتم بناؤها كيميائيًا لتسليم البضائع إلى داخل الخلايا بأرقى طريقة ممكنة وأكثرها قابلية للتحكم.
وقد طور العلماء في جامعة مونستر (بألمانيا) مؤخرًا نوعًا جديدًا من الحاويات النانوية التي تم إنشاؤها بالكامل من مكونات بيولوجية. وعلى عكس ناقلات البضائع الأخرى، فهذه لا تعتمد على الليبيدات ولكن على مركبات السكر التي يتم غلقها بقشرة من الهياكل البروتينية – ما يسمى بالبولي ببتيدات – التي يتم تفصيل سمكها بدقة. ويوضح الكيميائي البروفيسور بارت جان رافو: “نحن ننتج مكونات حاويات النانو الخاصة بنا صناعياً، ولكن تمتص من قبل الخلايا، وبسبب البنية الكلية التي طورناها تتحلل أيضًا بها تمامًا مثل المواد التي تحدث بشكل طبيعي”. ويضيف عالم الكيمياء الحيوية البروفيسور فولكر غيرك: “من أجل تحلل قشرة الحاوية داخل الخلية، نستخدم آليتين تحدثان بشكل طبيعي، ويتم نتيجة لذلك إفراغ المواد المنقولة بسرعة بمجرد وصولها إلى الخلية”.
ويريد العلماء استخدام الحاويات النانوية الصغيرة، التي يبلغ قطرها حوالي 150 نانومتر، لتحميل الخلايا بالدهون ذات الصلة بيولوجيًا والتي يمكن استخدامها لدراسة عمليات النقل التي تحدث داخل غشاء الخلية. ويخططون بالإضافة إلى ذلك لتطوير التصميم الكيميائي للحاويات بطريقة تجعلهن – على سبيل المثال – لا يتم تناولهن إلا من قبل أنواع معينة من الخلايا أو يطلقن حمولتهن فقط عند تحفيزهن بواسطة الضوء الخارجي. وفي المستقبل، قد تكون أنظمة النقل المبنية من مكونات السكر والبروتين مناسبة أيضًا للتطبيقات في الكائنات الحية لتوصيل الأدوية على وجه التحديد إلى أنسجة وخلايا معينة. وقد نُشرت الدراسة في مجلة “العلوم المتطورة” (Advanced Science).
المواد المستوحاة حيويا تنظم نفسها مشكِلَةً حاويات تحمل البضائع
لتجميع ناقلات البضائع الجديدة، استخدم العلماء مركبات السكر ( الديكسترينات الحلقية المعدلة ) التي تشبه في التركيب – وبالتالي السلوك – دهونًا معينة موجودة بشكل طبيعي في كل خلية. وعلى غرار دهون غشاء الخلية الواقية، ترتب هياكل السكر نفسها، وتشكل قشرةً يحيط فيه المواد المراد نقلها. ولكن نظرًا لأن الحاوية الناتجة لا تزال مسَرِّبة وستفقد حمولتها بمرور الوقت، أضاف العلماء هياكل بروتينية (عديد الببتيدات) تشكل طبقة مانعة للتسرب حول الحاوية. ويوضح شرفوضين پوتانام تشالي، طالب مرحلة الدكتوراه في الكيمياء وأحد المؤلفين الرئيسيين للدراسة: “لاختبار مقدار السماكة اللازمة للطبقة المانعة للتسرب، غيرنا بتفاوت طول سلاسل الببتيد وصممناها بحيث تغلف الحاوياتُ حمولتها بشكل مستقر”.
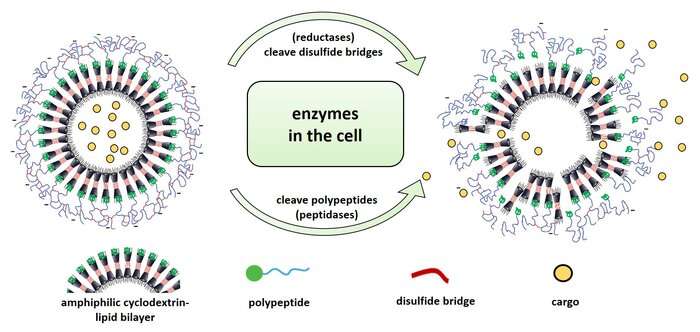
حاويات نانوية تستخدم مسارًا طبيعيًا إلى الخلايا
درس العلماء في الخطوة التالية ما إذا وكيف أُخِذت الحاويات النانوية المطورة حديثًا بواسطة الخلايا. وكانت فرضيتهم أن هذا يحدث عن طريق ما يسمى بالالتقام الخلوي. وفي هذه العملية، تستوعب الخلايا جزءً من غشاء الخلية وتقرصه، مخلقة حويصلات صغيرة تسمى الجسيمات الداخلية التي يتم فيها نقل المواد من خارج الخلية الى الخلية. ولاختبار ذلك، استخدم العلماء مركب سكر (ديكستران)، معروفٌ أنه يتم تناوله عن طريق الالتقام الخلوي. وقد عالجوا مزارعهم الخلوية باستخدام ديكستران فلوري أحمر، وفي نفس الوقت، أضافوا حاويات نانوية مملوءة بشحنة فلورية خضراء (البيرانين). ويشرح سيرجيج كودروك، طالب الدكتوراه في الكيمياء الحيوية ومؤلف رئيسي للدراسة: “في المجهر الضوئي، أصبح مرئيًا ان كلتا المادتين قد تم تناولهما في الخلايا بالتساوي وتداخل استشعاعهما بشكل واضح – لذلك يمكننا أن نستنتج أن الحاويات النانوية، تمامًا مثل الديكستران، تم امتصاصها بكفاءة من قبل الخلايا من خلال عملية النقل داخل الجسم”.
قشرة الحاوية تتحلل بفعل الانزيمات في داخل الخلايا
تختلف الظروف داخل الجسيمات الداخلية عن تلك الموجودة في البيئة الخلوية، وهو الأمر الذي كان العلماء يفكرون فيه بالفعل عند تصميم الحاويات النانوية الخاصة بهم. وقد أنشأوا الحاويات بطريقة أن البيئة المتغيرة في الجسيمات داخل الخلية تزعزع الاستقرار وتحلل جزئيا قشرة البولي ببتيد – ولهذا تصبح الحاويات النانوية مسرِبة وتفرغ حمولتها الى داخل الخلية. ويوضح سيرجيج كودروك: “عندما يتم أخذ الحاويات الى الجسيمات الداخلية، يأتي دور نوعين من الإنزيمات، التي عرفنا أنها موجودة في الجسيمات الداخلية والتي يمكن أن تسهم في تدهور القشرة في مواقع محددة”. ويضيف شرفوضين بوتانام تشالي: “تقوم ما يسمى مختزلات بتحليل جسور ثاني الكبريتيد التي أنشئت سابقا لربط جزيئات الببتيد في الحاويات النانوية لدينا – بالإضافة الى ذلك، تشق الببتيدات جزيئات الببتيد”. وقد اختبر العلماء أيضًا قابلية تحلل قشرة الحاوية خارج الخلية. وللقيام بذلك، قاموا بتحميل الحاويات بصبغة فلورية وجزء محاكاة من البيئة الدقيقة المعقدة داخل الجسم باستخدام إنزيم التربسين وكذلك عوامل الاختزال. وبعد العلاج، تسربت الصبغة للخارج على الفور.
*تمت الترجمة بتصرف
المصدر:
https://phys.org/news/2021-08-newly-bioinspired-cell-delivery-vehicles.html
لمزيد من المعلومات: سيرغيج كودروك وآخرون، Biodegradable and Dual‐Responsive Polypeptide‐Shelled Cyclodextrin‐Containers for Intracellular Delivery of Membrane‐Impermeable Cargo, Advanced Science (2021). DOI: 10.1002/advs.202100694

 علوم القطيف مقالات علمية في شتى المجالات العلمية
علوم القطيف مقالات علمية في شتى المجالات العلمية