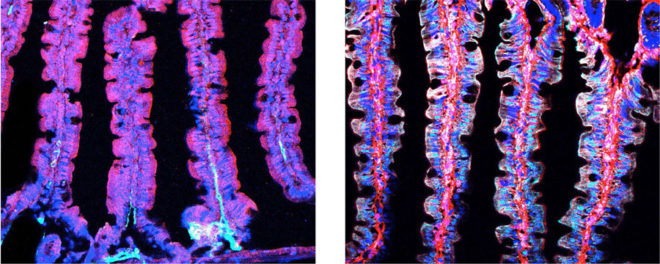
Why gut bacteria are becoming key suspects in autoimmune diseases
(بقلم: إيان جليليو، هورايزن، المجلة الاوروبية للبحوث والابتكار)
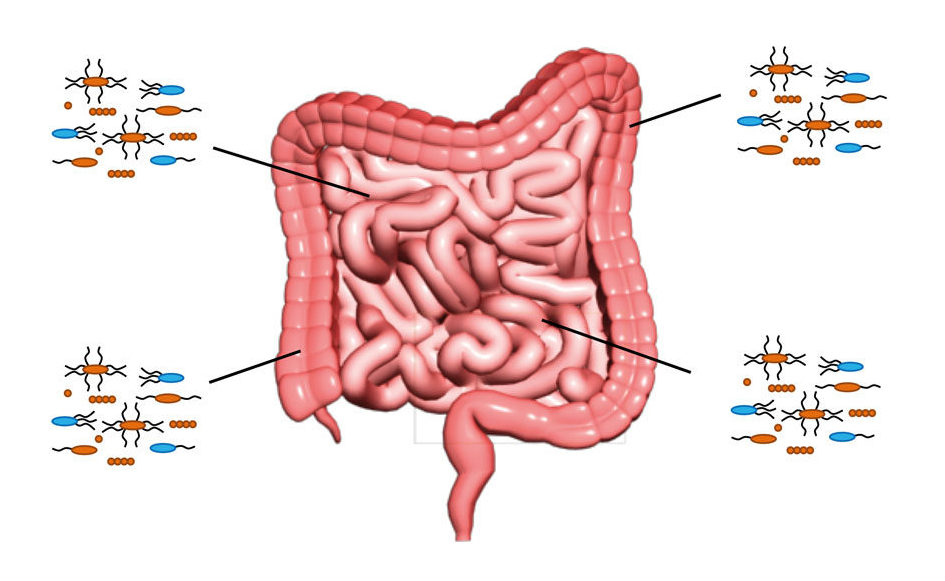
جهاز المناعة البشري قوي ومعقد. ويجب أن يكون على أهبة الاستعداد في جميع الأوقات وأن يكون قادرًا على التمييز بين الصديق والعدو. لسوء الحظ، قد يخطء الهدف في بعض الأحيان ويهاجم خلايا الجسم نفسه، مما يؤدي إلى مئات من أمراض “المناعة الذاتية”، من التصلب المتعدد (MS) إلى التهاب المفاصل الروماتزمي.
الأسباب التي تجعل جهاز المناعة يخطئ بهذه الطريقة لا زالت غير واضحة ، لكن مجموعة متنامية من الأبحاث تبحث في تريليونات الميكروبات التي تشاركنا أجسامنا، والمعروفة مجتمعة باسم الميكروبيوم ، كإحدى الإجابات.
الدراسات التي أجريت على التوائم تشير إلى أن نمط الحياة أو العوامل البيئية يمكن أن تلعب دورًا كبيرًا في أمراض المناعة الذاتية.
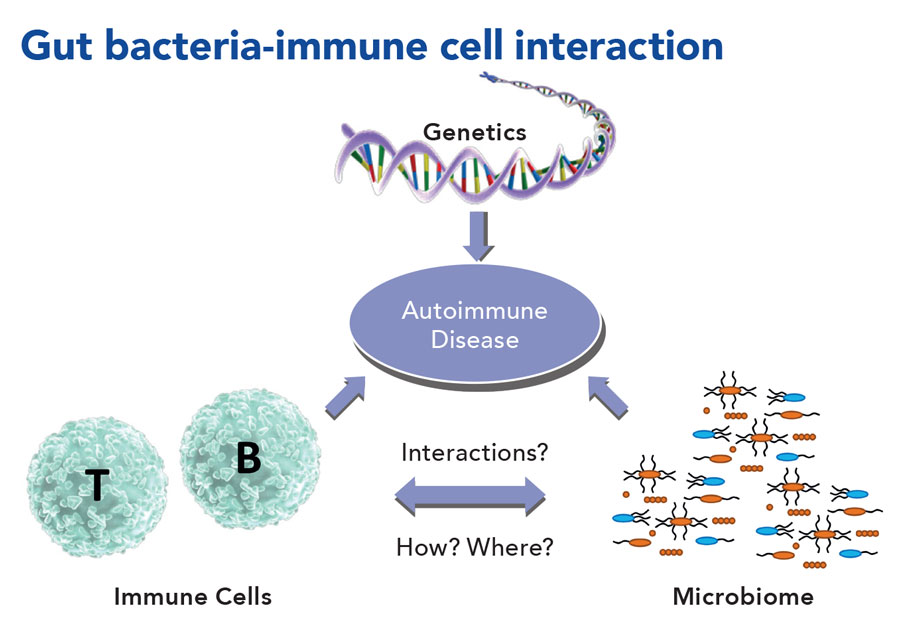
“لو نظرت فقط إلى معدل التوافق في التوائم (حيث يظهر على كلا التوأمين نفس السمة) ، على سبيل المثال بالنسبة لمرض التصلب العصبي المتعدد، فإن حوالي 30٪ فقط منها موروثة. “لذلك لا بد أن يكون الباقي منها يرجع إلى العوامل البيئة”، كما قال البروفسور ماركوس كلاينويتفيلد (Markus Kleinewietfeld) من معهد ڤي آي بي (VIB) في بلجيكا.
يُشتبه في أن العديد من العوامل البيئية المختلفة تؤثر على احتمال الإصابة بأمراض المناعة الذاتية، بما في ذلك النظام الغذائي.
الملح
وجد بحث سابق (2) أجراه البروفسور كلاينويتفيلد وآخرون أن الغذاء الغني بالملح يمكن أن يؤثر على جهازنا المناعي، بما في ذلك الخلايا المسؤولة عن الالتهابات. تعد الالتهاب جزءًا لا يتجزأ من الدفاع ضد العدوى (infection)، إلا أنه يمكن أن يتسبب في تلف الأنسجة والأعضاء حين تكون مستويات الاصابة بها مرتفعة.

الجهاز المناعي متوازن بعناية بين الخلايا التي تسبب الالتهاب والخلايا التي تنظم هذه الخلايا [المسببة للالتهاب]. البروفسور كلاينويتفيلد يتوقع أن الغذاء قد يخل بهذا التوازن، جزئيًا على الأقل، سواء بشكل مباشر من خلال التأثير على الخلايا المناعية المختلفة أو بشكل غير مباشر وذلك بتعديل ميكروبيوم الأمعاء.
“أردنا تحليل كيف يمكن أن تؤثر العوامل الغذائية المحددة على ميكروبيوم الأمعاء وقد تتلازم مع التحولات في جهاز المناعة”، كما قال البروفسور كلاينويتفيلد، الذي يقود مشروع (ENVIROIMMUNE) للتحقيق في تأثيرات الملح (2).
“ما وجدناه بالفعل، والذي كان مفاجئًا جدُا، هو أن (الغذاء الغني بالملح) يستنفد على وجه التحديد الميكروبات المفيدة ، مثل العصيات اللبنية (lactobacilli)، في الأمعاء”.
العصيات اللبنية هي نوع شائع من البكتيريا “النافعة (الصديقة)” الموجودة في الأمعاء. هناك العديد من أنواع العصيات اللبنية ، بما فيها بعض الأنواع المستخدمة في الإنتاج التجاري للزبادي والجبن والملفوف المخلل.
“لقد أجرينا أيضًا دراسة تجريبية صغيرة على البشر، وكان ذلك أيضًا مذهلاً للغاية لأننا لاحظنا نفاد (العصيات اللبنية)” ، كما قال البروفسور كلاينويتفيلد.
في غضون أيام قليلة، تمكن الباحثون من مشاهدة الاختلافات (3) في الذين تناولوا ستة غرامات إضافية من الملح يوميًا. لم يكن لديهم ارتفاع في ضغط الدم فحسب ، بل كان لديهم المزيد من الخلايا المناعية المسببة للالتهابات وعدد أقل من العصيات اللبنية.
المستقلبات
عند الفحص الدقيق، يبدو أن العصيات اللبنية تساعد في إبقاء الجهاز المناعي تحت السيطرة وذلك بإفراز مركبات تعرف باسم المستقلبات (4) – نواتج ثانوية لنشاط هذه البكتيريا.
يمكننا أن نظهر أن هذا التأثير (الزيادة في الخلايا المناعية المسببة للالتهابات) يعتمد على الأرجح على التحولات في المستقلبات التي تنتجها العصيات اللبنية ، لأن لها تأثيرًا مثبطًا في أنابيب الاختبار (in vitro) على الخلايا المناعية. قال البروفيسور كلاينويتفيلد: “فإذا كان لديك قليل من العصيات اللبنية ، فإن هذا التأثير التثبيطي يختفي”.

لا يزال هذا البحث في مراحله الأولى، وهناك حاجة إلى مزيد من العمل لمعرفة الآثار طويلة الامد للغذاء الغني بالملح على الميكروبيوم. تم إجراء هذه الدراسات على متطوعين أصحاء، ولذلك من الضروري اجراء اختبار بدقة على التأثير الذي يمكن أن يكون للتغييرات في الغذاء على مرض معين.
ومع ذلك، فإن دراسة الميكروبيوم تعطي أيضًا قرائن على أسباب أمراض مناعة ذاتية ليس لها أي علاج. أحد الأمثلة على ذلك هو التهاب الأقنية الصفراوية المصلب الأولي (PSC) (انظر 5). يتسبب هذا المرض النادر في حدوث انسداد في القنوات الصفراوية، مما يؤدي بدوره إلى تلف الكبد.
“إنه أمر محبط جدًا حيث لا يوجد لدينا علاج لهذا المرض سوى زراعة كبد” ، كما قال الدكتور يوهانس هوڤ (Johannes Hov) من جامعة أوسلو في النرويج. “وهذا في الواقع هو المؤشر الأكثر شيوعًا لزراعة الكبد في النرويج”.
الأمعاء
سبب المرض غير واضح ، ولكن هناك قرائن تشير إلى وجود صلة بين المناعة الذاتية والتغيرات في الميكروبيوم. يعاني العديد من مرضى التهاب الأقنية الصفراوية المصلب الأولي (PSC) من أمراض مناعة ذاتية أخرى ، كما أن بعض الجينات المرتبطة بالحالة المرضية مرتبطة أيضًا بالمناعة الذاتية. على وجه الخصوص ، هناك ارتباط قوي بالأمعاء. ما يصل إلى 80 ٪ من المرضى يعانون أيضًا من مرض الأمعاء الالتهابي (6).
“هذا يوحي لنا أن شيئًا ما يحدث في الأمعاء هام للمرض في الكبد، وهذا يشير بالفعل إلى الميكروبيوم كمسبب متهم” ، كما قال الدكتور هوف، الذي يقضي نصف وقته في البحث عن أسباب المرض والنصف الآخر في علاج المرضى في المستشفى.
وجدت الدراسات السابقة (7) على البكتيريا في أمعاء مرضى التهاب الأقنية الصفراوية المصلب الأولي (PSC) اختلافات مقارنةً بالأصحاء.
“إذن هذه هي نقطة البداية ؛ كون الميكروبيوم مختلفًا، لكننا لا نعرف في الحقيقة ما إذا كان هذا يسبب المرض ، أو ما إذا كان ناتجًا من المرض” ، كما قال الدكتور هوڤ.
إجابة جزئية على هذا السؤال يمكن أن تأتي من دراسة الأشخاص بعد اجراء زرع الكبد لهم. إذ حوالي ثلث مرضى التهاب الأقنية الصفراوية المصلب الأولي (PSC) يصابون بالمرض مرة أخرى في غضون بضع سنوات، مما يؤدي إلى تراكم الأضرار (التلف) في الكبد المزروعة.
“أعتقد أن هذا إثبات قوي إلى حد ما على أن هناك شيئًا ما يأتي من خارج الكبد ويهاجم الكبد”. “إنها في الحقيقة فرصة فريدة لمتابعة المرض من بدايته”.
أحد الاقتراحات بشأن السبب هو تسرب المستقلبات الميكروبية إلى مجرى الدم ، والتي تنتقل مباشرة من الأمعاء إلى الكبد. ومع ذلك، فإن معرفة أي المستقلبات تتسبب في المرض تعتبر مهمة صعبة ؛ يصف الدكتور هوڤ ميكروبيوم الأمعاء على أنه “مصنع كيميائي حيوي”.
في مشروع (StopAutoimmunity) (انظر 8)، يستخدم دكتور هوڤ مئات العينات جمعت على مر السنين من المرضى الذين يعانون من عودة المرض ومقارنتها بأولئك الذين عولجوا بزرع الكبد لهم.
يقوم الدكتور هوڤ بفحص عينات الدم لآلاف من المستقلبات المختلفة لمعرفة أي الأنماط مرتبطة بالمخرجات العلاجية. من تحليل عينات المرضى قبل الزرع ، وجد الدكتور هوڤ بالفعل تغييرات كبيرة في كيف تقوم الميكروبات باستقلاب بعض العناصر الغذائية الأساسية، بما في ذلك بعض الأحماض الأمينية وفيتامينات B.
“لذلك فإننا نتوقع بناءً على ذلك ، أن التغييرات في الميكروبيوم تقلل بطريقة ما من الاستفادة من العناصر الغذائية الأساسية، والتي من الممكن أن تؤثر على أمراض الكبد”.
زراعة البراز
لو وجد الباحثون مستقلبًا مسببًا لمرض ما، يأمل الدكتور هوڤ أن يتمكنوا من بدء محاولة تجريبية لاختبار علاجات، كالبروبيوتيك أو زرع البراز ، لتغيير توازن ميكروبات الأمعاء.
يمكنك فعل شيء باستخدام الميكروبيوم: يمكنك تغييره ، وربما معالجته. لذلك إذا كان لديك مرض ليس له علاج ، يعتبر الميكروبيوم بداية جيدة للبحث فيه عن العلاج”.
هذا هو الأمل الذي يدفع بمزيد من الباحثين لدراسة دور الميكروبيوم في الأمراض. ولكن ، مزيج مجموعات الميكروبات التي في أجسامنا معقدة ومتغيرة. حتى لو تمكن باحثون مثل البروفسور كلاينويتفيلد والدكتور هوڤ من تحديد الآليات المسؤولة عن النتيجة غير المرغوب فيها، فإن التحدي يظل متمثلًا في كيف يتم معالجتها بشكل موثوق. يمكن أن توفر امكانية التلاعب بالميكروبيوم طريقة لعلاج العديد من الحالات المرضية ، لكننا ما زلنا في البداية.
“أعتقد أن هناك الكثير سيأتي في المستقبل”. “لكننا بدأنا للتو في فهم كيف نستخدم هذه المعرفة بطريقة علاجية”.
مصادر من داخل وخارج النص:
1- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3746493/
2- https://cordis.europa.eu/project/id/640116
3- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6070150/
4- https://ar.wikipedia.org/wiki/مستقلب
5- “التهاب الأقنية الصفراوية المصلِّب الأوَّلي هو مرض يصيب القنوات الصفراوية. تحمل القنوات الصفراوية العصارة السائلة الهضمية من الكبد إلى الأمعاء الدقيقة. في حالة التهاب الأقنية الصفراوية المصلِّب الأوَّلي، يؤدي إلى حدوث ندبات داخل القنوات الصفراوية. وهذه الندبات تؤدي إلى تصلُّب وتضيق القنوات، وتؤدي إلى تلف الكبد بشدة تدريجيًا. يصيب داء الأمعاء الالتهابي أيضًا معظم الأشخاص المصابين بالتهاب القنوات الصفراوية المصلِّب الأوليّ، مثل التهاب القولون التقرحي أو داء كرون”، مقتبس من نص ورد على هذا العنوان:
https://www.mayoclinic.org/ar/diseases-conditions/primary-sclerosing-cholangitis/symptoms-causes/syc-20355797
6. ” أمراض الأمعاء الالتهابية (Inflammatory bowel disease) هي مجموعة من الأمراض الالتهابية التي تصيب الجهاز الهضمي، خاصّة القولون و الأمعاء الدقيقة. تتضمن مجموعة من الأمراض أهمها داء كرون و التهاب القولون التقرحي. من الضروري إدراك أن داء كرون لا يصيب القولون و الأمعاء الدقيقة فقط، إنما يمكن أن يُصيب الفم والمريء والمعدة و حتى فتحة الشرج أيضاً”، مقتبس من نص ورد على هذا العنوان: https://ar.wikipedia.org/wiki/داء_الأمعاء_الالتهابي ، https://cordis.europa.eu/project/id/802544
7- https://pubmed.ncbi.nlm.nih.gov/26887816/
8- https://cordis.europa.eu/project/id/802544

 علوم القطيف مقالات علمية في شتى المجالات العلمية
علوم القطيف مقالات علمية في شتى المجالات العلمية